成人高考
最新文章
- 1第七届教学督导团开始履职

第七届教学督导团开始履职 窦贤康希望督导......
- 2国际顶级期刊发表我校植物干
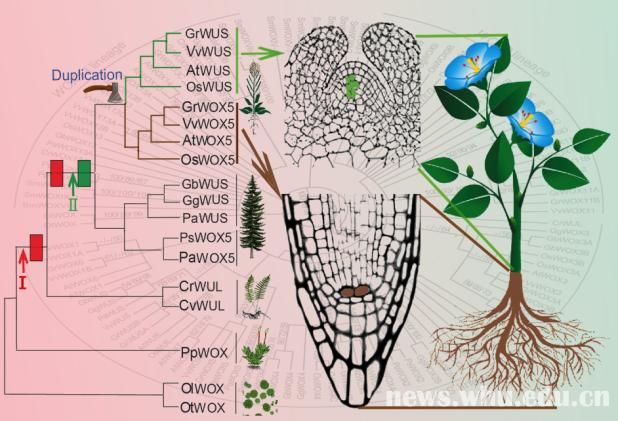
国际顶级期刊发表我校植物干细胞研究新成果......
- 3分子生物学与遗传学首次进入
分子生物学与遗传学首次进入ESI全球排名前1......
- 4亚洲地理信息体系大会李德仁

亚洲地理信息系统大会李德仁院士作主题报告......
- 5首届本科良好教学业绩奖450余
首届本科优秀教学业绩奖450余万元奖励一线教......
推荐文章
热门文章
- 1佳节将至送温暖

佳节将至送温暖 发布时间:2017-01-240...
- 2教育部政策法规司孙宵兵司长一行

本网讯(通讯员毛俊华/文王军/图)6月30日...
- 3CHINA DAILYFoothold strengthen

ByZhaoXinying(ChinaDaily) 编者按:...
- 4珞珈讲坛爱尔兰院士莫兰带你了解

本网讯(实习生卿青)12月12日,国际哲学联合会...
- 5亚洲地理信息体系大会李德仁院士

亚洲地理信息系统大会李德仁院士作主题报告...

